FUNDAMENTOS
La espectroscopia ultravioleta-visible o espectrofotometría
ultravioleta-visible (UV/VIS) es una espectroscopia de emisión de fotones y una
espectrofotometría. Utiliza radiación electromagnética (luz) de las regiones
visible, ultravioleta cercana (UV) e infrarroja cercana (NIR) del espectro
electromagnético, es decir, una longitud de onda entre 380nm y 780nm. La
radiación absorbida por las moléculas desde esta región del espectro provoca
transiciones electrónicas que pueden ser cuantificadas.
La espectroscopia UV-visible se utiliza para identificar algunos grupos funcionales de moléculas, y además, para determinar el contenido y fuerza de una sustancia.
Se utiliza de manera general en la determinación cuantitativa de los componentes de soluciones de iones de metales de transición y compuestos orgánicos altamente conjugados.
Se utiliza extensivamente en laboratorios de química y bioquímica para determinar pequeñas cantidades de cierta sustancia, como las trazas de metales en aleaciones o la concentración de cierto medicamento que puede llegar a ciertas partes del cuerpo.
Las moléculas orgánicas
distribuyen sus electrones en diferentes niveles electrónicos llamados
orbitales moleculares. Los orbitales moleculares de menor energía son los σ, a
continuación siguen los orbitales π. Cuando en la molécula existen átomos con
pares electrónicos libres (oxígeno, azufre, nitrógeno, halógenos) tendremos
niveles no enlazantes n. Estos niveles electrónicos se disponen en la región
enlazante del diagrama. En la región antienlazante nos encontramos con los
orbitales moleculares π∗ y σ∗. Una molécula en su
estado fundamental tiene ocupados los orbitales enlazantes y no enlazantes y
desocupados los antienlazntes.
De lo comentado
anteriormente se deduce que las transiciones electrónicas deben partir de los
orbitales enlazantes y no enlazantes terminando en los antienlazantes. Así
podemos tener los 5 tipos de transiciones electrónicas que se muestran en el
siguiente diagrama.
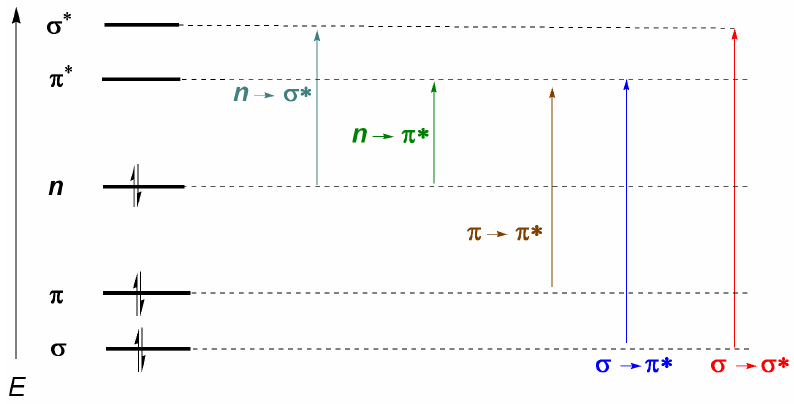
La transición electrónica
más importante suele ser del HOMO (último orbital ocupado) al LUMO (primero
orbital vacío) que corresponde al menor salto energético y le corresponde una
longitud de onda grande.
En los alcanos solo son
posibles transiciones σ→σ∗
(etano: λ=135nm). Estas bandas no pueden ser observadas con los
espectrofotómetros comerciales, puesto que hacen barridos a partir de los 200
nm. Sin embargo, las moléculas que presentan dobles enlaces conjugados
presentan transiciones π→π∗ que
pueden ser observadas (butadieno: λ=217nm).
Cuando en la molécula
existen átomos con pares libres, la transción de menor energía(mayor logitud de
onda) es n→π. Sin embargo, se trata de una transición poco probable, debido a
que no existe solapamiento entre ambor orbitales, originando bandas muy
débiles. De este último comentario se deduce la regla de selección de la
espectroscopía visible-UV: las transiones n→π∗ están
"prohibidas". Entendiéndose por prohibida una transición de baja
probabilidad.
Alcanos. Sus bandas de
absorción son debidas a transiciones σ→σ∗ de enlaces C-C y C-H. Estas transiciones son
de elevada energía y tienen lugar a longitudes de onda inferiores a los 150 nm,
no observables por tanto en espectrofotómetros convencionales. Esta
característica permite utilizarlos como disolventes de la muestar a anlizar, ya
que no interfieren con sus señales.
Alquenos y alquinos.
Presentan bandas de absorción debidas a las transiciones π→π∗ del triple enlace
C-C. Esta transición es de menor energía que en el caso de los alcanos y
aparece a longitudes de onda mayores (alquenos:175 nm; alquinos: 170 nm). El
doble y triple enlace son los grupos cromóforos de estas moléculas.
Éteres, tioles, sulfuros,
aminas: En este caso el grupo cromóforo está formado por el heteroátomo (O,S,N)
y los átomos que le enlazan. El heteroátomo presenta pares libres y la
transición que produce la absorción es n→σ∗. Esta banda de absorción aparece sobre
175-200 nm para alcoholes, éteres y aminas, desplazándose a 200-220 nm para los
sulfuro.
Aldehídos, cetonas, ácidos y
derivados. El grupo cromóforo de estos compuestos es el carbonilo (C=O). Dado
que el oxígeno posee pares libres, la transición de menor energía es la n→π∗, pero es una
transición prohibida (ϵmax=15),
al no existir solapamiento entre los orbitales implicados. La siguiente
transición de menor energía es la π→π∗,
observable a λmax=188nm, con absortividad molar de 900.
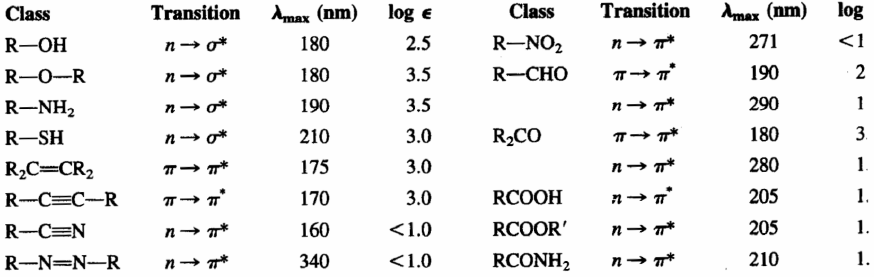
En la siguiente tabla se
indican las absorciones de los principales grupos cromóforos.
Deben estudiarlo para el día martes
Rafael Troche
Docente Análisis Instrumental
No hay comentarios:
Publicar un comentario