EL COLOR
El mundo que conocemos se ve muy bien a colores. A todos nos gusta contemplar los campos verdes, el cielo azul o las flores de diferentes colores. Pero no solo la naturaleza es colorida. Nos gustan tanto los colores que los queremos capturar en nuestros objetos; deseamos pintar nuestras casas, teñir nuestra ropa, imprimir fotografías brillantes, tener una televisión a colores, comer alimentos de buen color.
El estudio de los colores ha sido muy profundo, sin embargo, como en cualquier área de las ciencias, siempre queda algo por hacer.
¿ Que es la Luz?
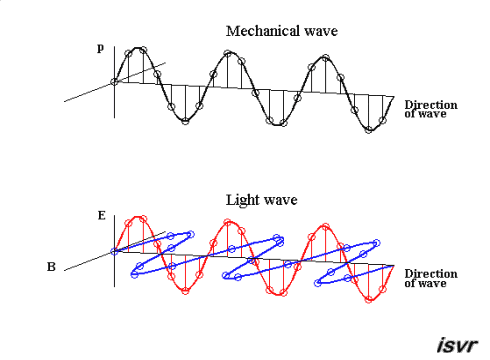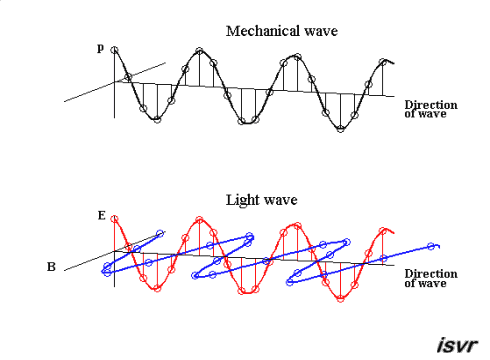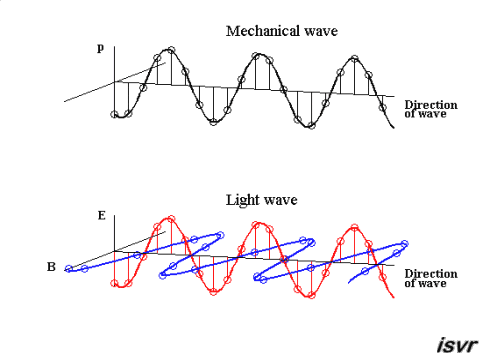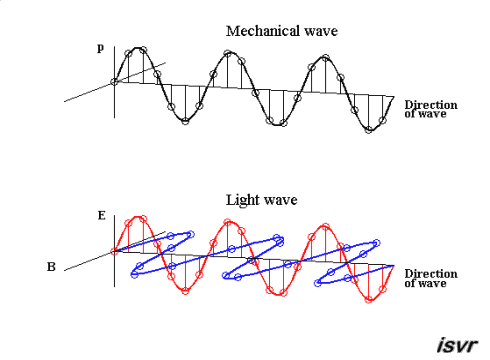
La luz visible para nosotros una parte muy pequeña del espectro electromagnético. La luz, un fenómeno complejo, está compuesto de fotones (del griego, φοος, luz) que tienen propiedades mecánico-ondulatorias, esto es: una propiedad de onda (como la de las olas en el mar) y una propiedad de partícula (como una canica diminuta), que llevan una energía definida.
Los diferentes tipos de radiaciones se dividen según su longitud de onda y son: ondas de radio (1Mm-30cm), microondas (30cm-1mm), infrarrojo (1mm-700nm), espectro visible (700nm-400nm), ultravioleta (400nm-10nm), rayos X (10nm-10pm), rayos gamma (γ, 10pm-1pm) y rayos cósmicos (1pm-1fm).
Es así que la longitud de onda se relaciona de manera inversamente proporcional con la energía.

Descomposición de la luz blanca.
Hay varias formas de producir colores: puede sr por descomposición de la luz blanca, por absorción de luz o por emisión de luz. En el primer caso no es muy importante con que sustancia esté interactuando la luz, pero en los dos últimos casos sí importa mucho la estructura atómica y molecular de la sustancia. ¿Porqué el cielo es azul? No es porque refleje el color del mar, sino por dispersión de la parte azul de la luz. Esto es provocado por un fenómeno llamado dispersión de Raleigh, que se manifiesta cuando una onda interactúa con una partícula que es menor de un décimo de su longitud de onda, es decir, al llegar a la luz del Sol a la Tierra, choca con las moléculas del aire de nuestra atmósfera, que son principalmente oxígeno (O2) y nitrógeno (N2); estas moléculas dispersan la luz azul con más fuerza y, en lugar de seguir su camino, se desvía y llega a nuestros ojos.
Absorción de luz.
Una sustancia puede absorber radiación si su energía corresponde exactamente a la necesaria para que suba a un nivel de mayor energía. Los fotones de la luz visible generalmente tienen la energía suficiente para que los electrones de una sustancia suban a un nivel más energético. Pero un electrón en un átomo o una molécula no tiene permitido absorber cualquier cantidad de energía. Como los fotones de luz de cada color tienen diferente energía, una sustancia puede absorber unos colores y otros no. Pensemos en una hoja de un árbol que todavía este verde: recibe luz blanca y nosotros la vemos verde. Esto significa que está llegando luz verde desde la hoja hasta nuestros ojos, pero la luz blanca es una mezcla de todos los colores, ¿qué les pasó a los demás colores si solo vemos el verde? La respuesta es que fueron absorbidos por la hoja; el verde no se absorbe y se refleja a nuestros ojos.
En el caso de las plantas, conocemos las estructuras de las moléculas más comunes que les dan color. Por ejemplo, el color verde es debido a la clorofila; algunos rojos y la mayor parte de los tonos de naranjado y amarillo se deben a moléculas conocidas como carotenoides, y muchos tonos del rojo, azul y morado son causados por las antocianinas.
Las plantas verdes deben su color a la gran cantidad de clorofila que tienen en sus hojas o tallos. Esta molécula es la encargada de absorber la luz que servirá como fuente de energía durante el proceso de fotosíntesis. Una parte muy importante en la estructura de la clorofila es el átomo central de magnesio (Mg), que le brinda muchas de sus propiedades y sin el cual no sería capaz de cumplir su función.
Los carotenoides están presentes en muchas frutas y verduras. Hay más de 700 carotenoides en la naturaleza y uno de los más conocidos es el beta-caroteno, la fuente de la vitamina A y una de las moléculas que le dan color a la zanahoria, el melón, el mango, pero también se encuentra en las espinacas y el brócoli. Nuestro cuerpo necesita vitamina A para fabricar el retinal que formará a la rodopsina que es indispensable en la percepción de la luz. Esa es una de las muchas buenas razones para consumir frutas y verduras.
Las antocianinas se encuentran, principalmente, en las flores y los frutos a los que imparten un amplio rango de colores. Hay más de 300 moléculas en este grupo. La col morada tiene muchos compuestos a los cuales debe su color tan intenso, básicamente antocianinas. Cuando estas antocianinas se someten a un cambio de pH cambian de color. Este cambio es provocado por una pequeña modificación en la estructura de la antocianina. Un ácido puede ceder un átomo de hidrógeno a la antocianina y una base puede quitarle uno; estas reacciones cambian su distribución de electrones y provocan un cambio de color. Muchos otros compuestos son capaces de cambiar de color al variar la concentración de hidrogeniones en la solución y se usan en química como indicadores.
¿A qué se debe el color rojo de la sangre? En nuestra sangre circulan muchas células conocidas como eritrocitos o glóbulos rojos, en los que hay una molécula muy grande que se encarga de transportar el oxígeno desde nuestros pulmones hasta todos los rincones de nuestro cuerpo: la hemoglobina. La hemoglobina es una proteína que tiene en su interior un fragmento conocido como grupo hemo, que es el causante de su color rojo, el cual tiene un átomo de hierro (Fe) en el centro del anillo de protoporfirina IX, encargado de unirse a la molécula de oxígeno. Si compramos la estructura de la clorofila con la del grupo hemo, notaremos un enorme parecido. El hecho de que una sea verde y el otro rojo se debe, principalmente al cambio de metal en el centro de la estructura.
Para los textiles se utilizaban tintes extraídos de plantas como el índigo, que da un tinte azul, o el palo de Brasil, para teñir de color rojo; otros eran extraídos de insectos, como el carmín, que es un colorante rojo extraído de la cochinilla del nopal, y el púrpura, un tinte extremadamente codiciado, usado solamente por la realeza y el clero, que era extraído de algunas especies de caracoles. Estas sustancias son compuestos orgánicos que no eran accesibles al público en general ya que su extracción era costosa. Hoy el mercado de los colorantes está dominado por los compuestos orgánicos sintéticos. La industria química ha desarrollado una amplia variedad de compuestos para usos muy específicos. Los más importantes son los tintes azo (caracterizados por tener dos nitrógenos unidos N=N), que corresponden a 60 ó 70% de los tintes utilizados en textiles; los tintes de carbonilo (caracterizados por tener un grupo carbonilo C=O), que son segundos en importancia y se adhieren mejor a textiles de algodón; las ftalocianinas (con estructura parecida a la clorofila o el grupo hemo), que son moléculas muy útiles para hacer tintas con colores intensos y duraderos, entre otros. Algunos compuestos inorgánicos son utilizados todavía y no difieren mucho de los usados desde hace cientos o miles de años, como los óxidos de hierro (FeO (OH), Fe2O3, Fe3O4), del cromato de plomo (PbCrO4) el sulfuro de cadmio (CdS), el ultramarino (Na8-10Al6Si6O24S2-4), el negro de humo, que es simplemente carbón y el azul de Prusia (Fe4 [Fe (CN)6]3), por mencionar los más importantes.
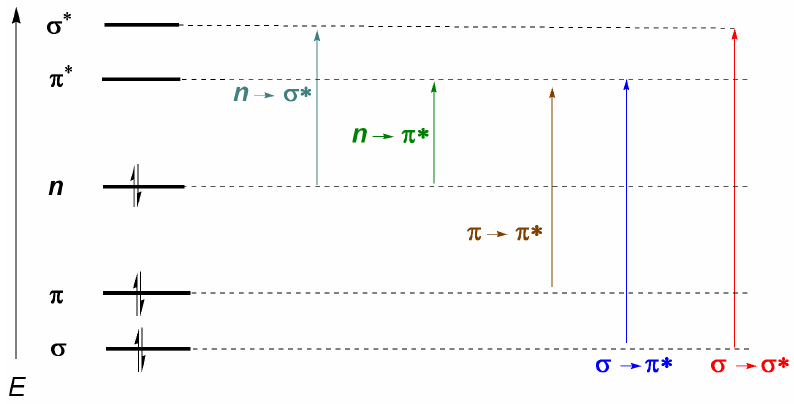
LAS TRANSICIONES ELECTRÓNICAS
Los átomos absorben luz de una longitud de onda pero inmediatamente liberan esta energía en forma de luz de otra longitud distinta. Esto es conocido como fluorescencia, y ocurre cuando un electrón toma energía, pasa a una órbita más elevada y luego cae otra vez en varios saltos. Muchas sustancias producen fluorescencia cuando la luz ultravioleta incide sobre ellas. No vemos el ultravioleta, pero podemos observar la energía de bajo nivel que produce.
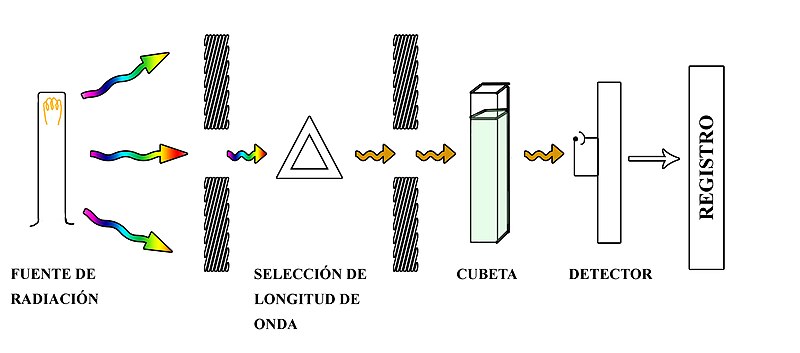
La cantidad de luz absorbida es proporcional al producto de la concentración, la longitud de paso óptico y el coeficiente de absortividad molar, que es la conocida ley de Lambert-Beer-Bouguer. La absortividad molar (ε) de un compuesto es una constante característica de ese compuesto a determinada longitud de onda. Como la absorbancia es proporcional a la concentración, se puede determinar la concentración de una disolución si se conocen la absorbancia y la absortividad molar a determinada longitud de onda. De ahí la importancia de esta ley, además de que nos muestra la interacción entre la materia y la energía en forma luminosa.
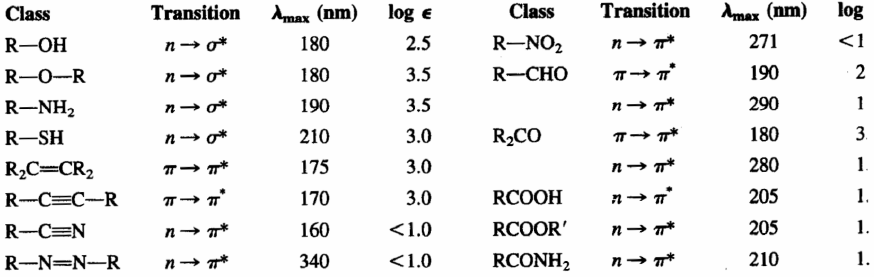
Efecto de la conjugación sobre la λmáx.
Mientras más enlaces dobles conjugados tenga un compuesto, la longitud de onda en la que suceden las transiciones n→π* y π→π* será mayor. Por ejemplo, la transición n→π* de la metilvinilcetona está a 324nm, y la transición π→π* está a 219 nm. Ambos valores son de longitudes de onda mayores que los correspondientes a las λmáx de la acetona porque la metilvinilcetona cuenta con dos enlaces dobles conjugados, mientras que la acetona solo tiene un enlace doble. La λmáx y la absortividad molar aumentan cuando aumenta la cantidad de enlaces dobles conjugados. Así, con la λmáx de un compuesto se puede estimar la cantidad de enlaces dobles conjugados que tiene el compuesto. Si un compuesto tiene los enlaces dobles suficientes absorberá luz visible y el compuesto tendrá color. Con esto en mente, el β-caroteno es una sustancia anaranjada y el licopeno, que se encuentra en jitomates, sandias y uvas rosadas es rojo.
Emisión de luz.
Veamos por último, la producción de colores por emisión de luz. Hay cosas que emiten luz colorida, como las lámparas de alumbrado público que emiten luz amarilla, los láseres o los LEDs de los semáforos modernos. En estos casos no hay absorción de luz de un color, simplemente se producen ciertos colores. El fuego es una reacción química muy vigorosa, es una oxidación muy rápida. En esta reacción se desprende mucha energía en forma de luz y calor. Hay reacciones de combustión que producen mucha luz, como es el caso de la combustión del magnesio metálico. La luz es tan intensa que es difícil mirar a la llama directamente sin lastimarse los ojos. Pero esta luz es casi de color blanco.
Los fuegos pirotécnicos son un espectáculo muy usado en ocasiones especiales. Es común celebrar la noche del 15 de septiembre con un castillo en el cual hay luces multicolores y tal vez hasta una bandera de México que se ilumina con la pólvora ardiente. Para lograrlo, se utilizan compuestos metálicos que se añaden a la pólvora y que, al arder, brillarán de un color en particular. Si se ponen sales metálicas en una llama, cada metal brillará con su color particular.
Es notorio el color tan característico e intenso que imparte el sodio a una llama. Cualquiera que haya cocinado, habrá visto que la sal de cocina (cloruro de sodio, NaCl) vuelve a la llama de color amarillo-naranja. Sí este color se parece al de las lámparas de alumbrado público no es una coincidencia. En el interior de estas lámparas se encuentra un poco de sodio metálico, que con el vapor se evapora fácilmente y brilla con gran intensidad. Estas lámparas son por mucho más efectivas en cuanto a producción de luz se refiere y su número es tan abundante en algunas ciudades que cuando está nublado de noche, las nubes presentan un ligero color naranja, que no es más que el reflejo de la luz producida por ellas.
Deben repasarlo para el día martes
Rafael Troche
Docente Análisis Instrumental